ATS
Avaliação de Tecnologias em Saúde (ATS): o que é?
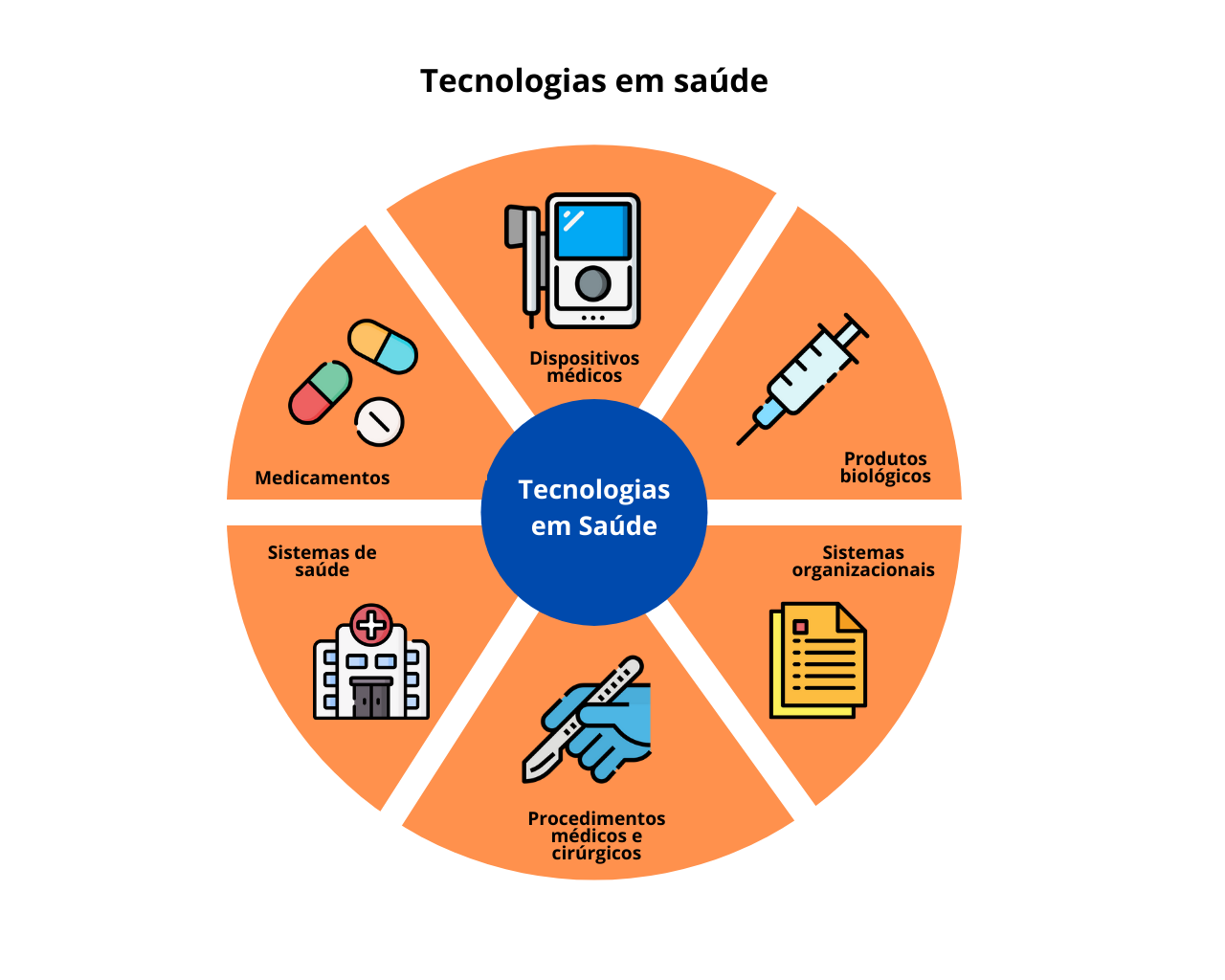
As tecnologias em saúde (como, por exemplo, medicamentos, produtos para a saúde, procedimentos, sistemas organizacionais, educacionais, de informação e de suporte e os programas e protocolos assistenciais por meio dos quais a atenção e os cuidados com a saúde são prestados à população) se refere à aplicação de conhecimentos com objetivo de promover a saúde, prevenir e tratar as doenças e reabilitar as pessoas. As tecnologias em saúde estão presentes desde a prevenção de doenças até o tratamento e recuperação da saúde das pessoas. A utilização correta das tecnologias em saúde e a atualização constante das informações sobre elas são imprescindíveis para um maior benefício para os pacientes e também para os seus cuidadores e familiares.
A avaliação das tecnologias em saúde (ATS) é um processo baseado em evidências que procura examinar as consequências da utilização de uma tecnologia de cuidados de saúde. Trata-se de um campo multidisciplinar de análise de políticas, que estuda as implicações clínicas, sociais, éticas e econômicas do desenvolvimento, difusão e uso da tecnologia em saúde.
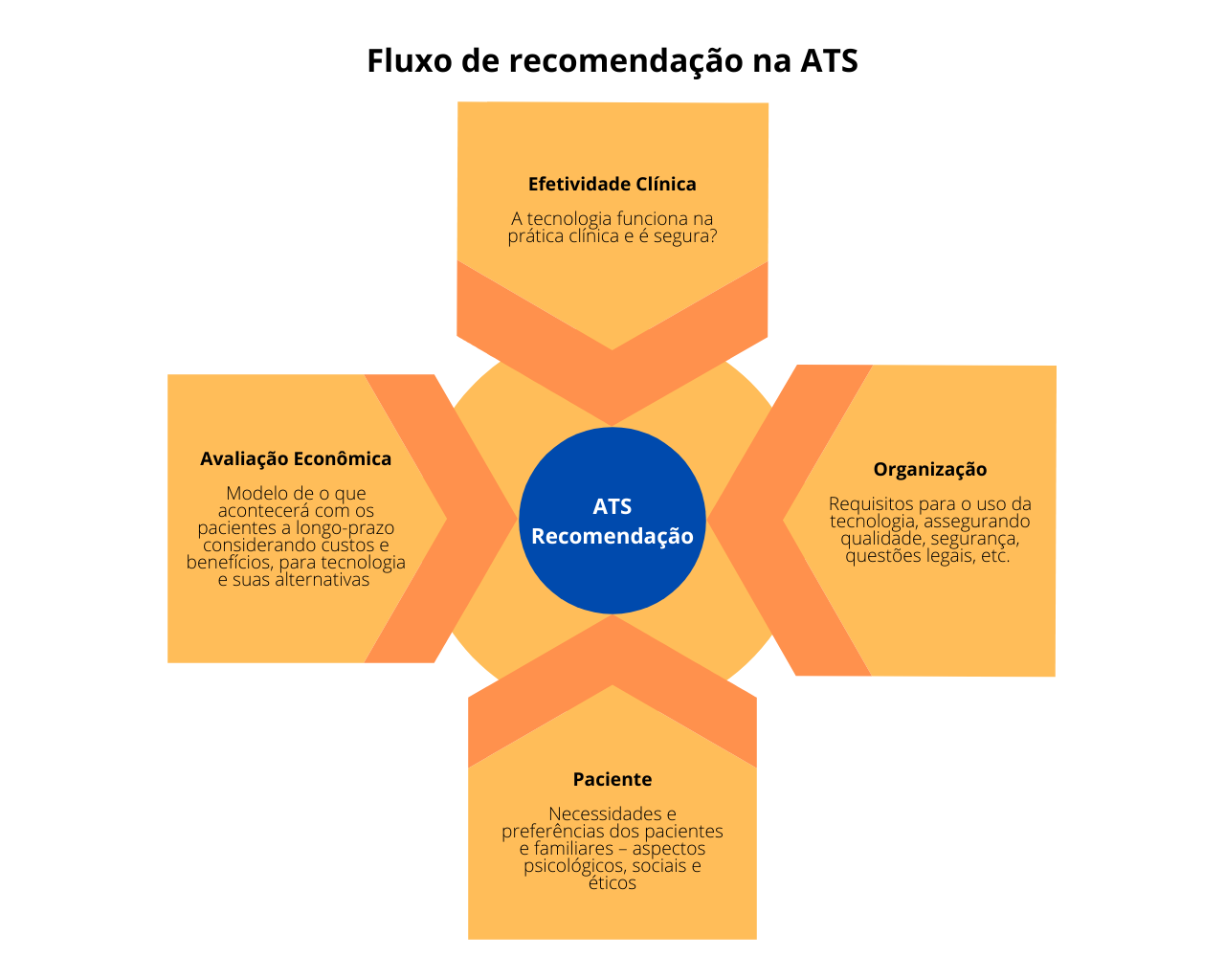
A ATS apoia decisões como:
• Para quais pacientes deve ser fornecido o tratamento?
• Por quanto tempo os pacientes devem receber o tratamento?

A ATS tem como objetivo fornecer aos tomadores de decisão informações quanto ao possível impacto e consequências de uma nova tecnologia em saúde ou de mudanças em uma tecnologia estabelecida. É responsável por avaliar as consequências diretas e indiretas, benefícios e desvantagens, e pelo mapeamento das etapas envolvidas em qualquer transferência de tecnologia, tanto no setor privado quanto público. Dessa forma, o papel da ATS é fornecer para os tomadores de decisão uma análise hierarquizada das opções de políticas de saúde, com um entendimento das implicações em saúde, econômicas, ambientais, sociais, políticas e legais para a sociedade.
Como se faz ATS?
A ATS surgiu na década de 1960 e destacou-se junto ao crescimento exponencial de tecnologias em saúde associadas a maior custo, rápida evolução e obsolescência. A ATS como atividade institucionalizada, cresceu nos países desenvolvidos a partir dos anos 1970, como parte da vigilância sanitária, estruturas públicas progressivamente mais poderosas, responsáveis pela análise de medicamentos, materiais e equipamentos entrantes no mercado, para serem usadas pela população e pelos serviços de saúde. Ao longo dos anos teve seu reconhecimento e escopo ampliados, incorporando e evoluindo método próprio e foco de atuação.
A ATS pode avaliar evidências científicas (estudos) provenientes de várias fontes, por exemplo:
- Estudos clínicos: estudos que estudam uma intervenção a fim de avaliar seus efeitos.
- Revisões sistemáticas de estudos clínicos: análise conjunta de diversos estudos que avaliam o mesmo efeito, permitindo análises em maior número e de maior confiança.
- Avaliações econômicas: estudos comparativos que analisam os valores dos recursos aplicados e dos resultados em saúde obtidos, ajudando nas decisões sobre o uso dos recursos.
ATS no Brasil
No Brasil, o processo de ATS se desenvolveu num ritmo mais acelerado a partir de 2004, quando da constituição do Departamento de Ciência e Tecnologia (DECIT) e aprovação da Política Nacional de Gestão de Tecnologias em Saúde. A Rede Brasileira de Avaliação de Tecnologia em Saúde (REBRATS) foi desenvolvida em 2007 para melhorar a capacidade de regulação do governo e com o intuito de definir critérios de prioridade e divulgar metodologia de estudos de ATS. Em 2011, a Lei nº 12.401, que altera a Lei nº 8.080 de 1990, regulamentada pelo Decreto nº 7.646 de 21 de dezembro de 2011, instituiu a criação da Comissão Nacional de Incorporação de Tecnologias no SUS (CONITEC). A partir daí a ATS passou a ser utilizada, com o respaldo da legislação, como ferramenta para subsidiar a tomada de decisão no âmbito do SUS.

Diferentes instituições e processos participam da ATS no Brasil. Uma síntese das instâncias e processos direcionados a avaliação e incorporação de tecnologias para o sistema de saúde no Brasil pode ser organizada da seguinte forma:
Aprovação para registro e comercialização:
ANVISA: autoriza o registro de um medicamento ou produto no Brasil
CMED: regula o preço de medicamentos no Brasil
Seleção para avaliação:
DECIT: sugere tecnologias para avaliação a partir de prospecção e critérios de priorização definidos com gestores e pesquisadores.
REBRATS: avalia a partir de monitoramento de tecnologias emergentes e agenda de pesquisa estratégica para o SUS.
CONITEC: define tecnologias para avaliação em função de demandas de incorporação recebidas e de ações judiciais
Avaliação:
REBRATS e CONITEC: buscam valorar sistematicamente as propriedades, efeitos ou impactos das tecnologias em saúde com o propósito principal de informar aos tomadores de decisão em saúde.
Deliberação:
CONITEC: acolhe os pontos de vista de todos os atores e especialistas no tema para fazer uma recomendação final, com base nisto e na evidência científica aportada pela avaliação de tecnologias em saúde.
Decisão:
SCTIE: decide quais tecnologias serão cobertas, em que condições e para quem, levando em conta o racional das recomendações e sua adequação com a política sanitária e sustentabilidade do sistema.
Apelação:
Qualquer instância demandante: dar oportunidade de manifestar-se a quem está em desacordo com o processo, antes da decisão finalizar.
Monitoramento e avaliação:
CONITEC: monitoramento do desempenho dos processos de incorporação
SECRETARIAS ESTADUAIS E MUNICIPAIS: revisa o cumprimento dos processos e dos resultados esperados do processo de priorização
REBRATS: pesquisa clínicas e pós implementação
A pesquisa em ATS no IATS
A concepção científica do IATS baseia-se em uma plataforma metodológica de apoio à pesquisa em ATS e monitoramento das tecnologias, incluindo pesquisas clínico-epidemiológicas, principalmente ensaios clínicos randomizados, revisões sistemáticas, metanálises e análises econômicas, inter-relacionados com agenda de pesquisa clínica a ser desenvolvida pelos núcleos de doenças cardiovasculares, diabetes e fatores de risco, doenças infecciosas, com ênfase em HIV/AIDS e hepatites, atenção primária em saúde, vacinas, oncologia, saúde mental e alta complexidade. Dessa forma, os projetos de pesquisa estão organizados a partir de seis eixos temáticos e seis eixos metodológicos.
Eixos temáticos
- Doenças Cardiovasculares e Fatores de Risco
- Hipertensão Arterial, Diabetes Mellitus, Obesidade, Terapias
- Doenças Infecciosas e Tropicais
- Vacinas e Imunopreviníveis
- Serviços de Saúde e Políticas Públicas
- Outras Doenças Não-Transmissíveis
Eixos metodológicos
- Plataforma Metodológica de Apoio à Avaliação e Monitoramento de Tecnologias em Saúde
- Pesquisas Epidemiológicas
- Ensaios Clínicos Randomizados
- Revisões Sistemáticas da Literatura
- Metanálises
- Análises Econômicas
Para saber mais
Fontes:
Brasil. Ministério da Saúde. Secretaria-Executiva. Área de Economia da Saúde e Desenvolvimento. Avaliação de tecnologias em saúde: ferramentas para a gestão do SUS Editora do Ministério da Saúde, 2009. 110 p. Link.
Brasil. Ministério da Saúde. Secretaria de Ciência, Tecnologia e Insumos Estratégicos. Departamento de Gestão e Incorporação de Tecnologias em Saúde. Entendendo a Incorporação de Tecnologias em Saúde no SUS: como se envolver. Brasília: Ministério da Saúde, 2016. 34 p. Link.
Experiências internacionais em Avaliação de Tecnologias Em Saúde: implicações para o Brasil. Coordenação: Carisi Anne Polanczyk. IESS e IATS, 2021. Link.
POLANCZYK, Carisi Anne; VIANNA, Denizar. Avaliação de Tecnologia em Saúde no Brasil. In: Saúde suplementar: 20 anos de transformações e desafios em um setor de evolução contínua. Coordenação e organização: José Cechin. Londrina: Midiograf, 2020. 418 p. Link.